L’étiquette d’un flacon porte les indications suivantes :
Solution pour rinçage de la verrerie de laboratoire.
Contient \({m_0} = 100g\) d'acide éthanoïque par litre de solution.
Afin de vérifier la masse mg d’acide éthanoïque \(C{H_3}COOH\) présente dans un litre de solution, on effectue les opérations suivantes :
1- Dilution :
On dilue au dixième la solution du flacon noté \({S_0}\) de concentration \({C_0}\) et on obtient \({V_1} = 100mL\) d’une solution \({S_1} = 100mL\) de concentration \({C_1}\) tel que \({C_1} = \frac{{{C_0}}}{{10}}\).
1-1- Déterminer le volume initial \({V_0}\) de la solution \({S_0}\) à prélever. 4 pt
1-2- On dispose des lots de verreries A ; B ; C ci-dessous :
Lot A
• Pipette jaugée de 10 mL
• Fiole jaugée de 100 mL
Lot B
• Éprouvette graduée de 10 mL
• Becher de 50 mL
Lot C
• Becher de 50 mL
• Burette graduée
Choisir le lot à utiliser 2 pt
1-3 Pour mesurer avec précision le volume \({V_0}\) indiquer parmi les trois positions de l’œil (voir figure ci-dessous), celle qui est correcte.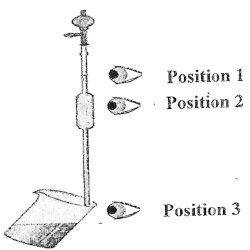 2- Titrage acido-basique :
2- Titrage acido-basique :
On réalise le titrage pH-métrique d’un volume \({V_1}\) = 10 mL de la solution \({S_1}\) diluée par une solution dihydroxyde de sodium \(\left( {N{a^ + } + H{O^ - }} \right)\) de concentration molaire \({C_2}\) = 0,10 mo1/L.
2-1- Citer deux éléments de verrerie à utiliser pour effectuer ce dosage. 2pt
2-2 A l’équivalence le volume de base versé est \({V_{2E}} = 17mL\):
2-2-1 Déterminer la concentration \({C_1}\) de la solution diluée sachant qu’à l’équivalence on a la relation \({C_1} \times {V_1} = {C_2} \times {V_{2E}}\) 3 pt
2-2-2 Verifier que \({C_0} = 1,7moL/L\) 2 pt
2-3- Déduire la masse mg d’acide éthanoïque présente dans un volume V= 1 L de solution. 2 pt
Masse molaire de \(C{H_3}COOH\) : M = 60 g/mol.
2-4- Dire si le dosage a permis de trouver une masse très proche a celle de l’étiquette. 1 pt
3- Donner une règle de sécurité à respecter au laboratoire de chimie. 2 pt


